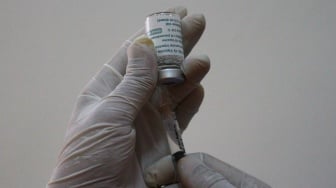
SuaraBali.id - Bahan baku vaksin Nusantara Terawan ternyata kebanyakan dari luar negeri atau impor. Sehingga tidak tepat jika vaksin Nusantara Terawan ini disebut asli Indonesia.
Hal itu dibongkar oleh Badan Pengawas Obat dan Makanan (BPOM).
BPOM menilai pengembangan vaksin dalam negeri ini tak memenuhi kaidah-kaidah dalam pembuatan vaksin.
Mengingat besarnya dampak pada kesehatan masyarakat luas jika akhirnya diedarkan secara luas, BPOM merasa penting untuk mengawasi secara ketat pengembangan semua vaksin, termasuk Vaksin Nusantara.
Baca Juga:Siti Fadilah Dukung Vaksin Nusantara, Begini Respon Epidemiolog
Selain itu, Vaksin Nusantara ternyata tak sepenuhnya vaksin buatan dalam negeri. Hampir Semua Komponennya Impor, seperti dilansir Solopos.com.
Komnas Penilai Khusus Vaksin Covid-19 dalam workshop di Jakarta baru-baru ini menyebut salah satu catatan untuk Vaksin Nusantara adalah antigen yang digunakan tidak diproduksi sendiri. Karenanya, relevansinya dengan strain Covid-19 yang ada di Indonesia, dipertanyakan.
![Peneliti Vaksin Nusantara di RSUP Kariadi Semarang [Suara.com/Dafi Yusuf]](https://media.suara.com/pictures/653x366/2021/02/19/99189-vaksin-nusantara.jpg)
"Kalau kita bicara Vaksin Nusantara, maka antigennya itu bukan dari virus Indonesia. Tapi didapatkan dari Amerika yang kita tidak tahu persis sebetulnya bagaimana sequence genomic-nya dan strain virus apa yang didapat dari Amerika," kata Dr dr Anwar Santoso, SpJP(K), Selasa (13/4/2021) lalu.
Dalam evaluasi uji klinis vaksin nusantara oleh BPOM, penggunaan komponen dari Aivita Biomedical Inc, perusahaan Amerika Serikat yang menyokong riset Vaksin Nusantara, juga menjadi salah satu catatan utama.
"Semua komponen utama pembuatan vaksin dendritik ini diimpor dari AS [meliputi antigen, GMCSF, medium pembuatan sel, dan alat-alat untuk persiapan]," tulis Kepala BPOM, Penny K Lukito dalam rilisnya, Rabu.
Baca Juga:Dinilai Tak Ikuti Aturan, Epidemiolog Minta Nama Vaksin Nusantara Diganti
Selain itu, untuk dilakukan transfer teknologi sehingga bisa dibuat di Indonesia, menurut BPOM bakal makan waktu sangat lama. Ini karena Aivita Biomedical Inc belum memiliki sarana produksi untuk produk biologi. Butuh 2-5 tahun untuk mengembangkannya di Indonesia.
"Berdasarkan penjelasan CEO AIVITA Indonesia, mereka akan mengimpor obat-obatan sebelum produksi di Indonesia," lanjut Penny.
Catatan lain yang disorot BPOM adalah data-data penelitian disimpan dan dilaporkan dalam electronic case report form, menggunakan sistem elektronik dengan nama redcap cloud yang dikembangkan Aivita Biomedical Inc dengan server di Amerika.

"Kerahasiaan data dan transfer data keluar negeri tidak tertuang dalam perjanjian penelitian, karena tidak ada perjanjian antara peneliti Indonesia dengan AIVITA Biomedical Inc USA," kata Penny.
BPOM juga mencatat keterlibatan peneliti asing dalam riset vaksin nusantara, sehingga dalam dengar pendapat dengan Komnas Penilai Obat ada banyak hal yang tidak bisa dijelaskan oleh peneliti utama dari Indonesia.
"Proses pembuatan vaksin sel dendritik dilakukan oleh peneliti dari AIVITA Biomedical Inc, USA, meskipun dilakukan training kepada staf di RS. Kariadi tetapi pada pelaksanaannya dilakukan oleh dari AIVITA Biomedica Inc, USA. Ada beberapa komponen tambahan dalam sediaan vaksin yang tidak diketahui isinya dan tim dari RS. Kariadi tidak memahami," tulis Penny.
BPOM menyebut, riset vaksin nusantara harus dikembangkan lagi di fase preklinik sebelum masuk ke uji klinik untuk mendapatkan 'basic concept yang jelas'.
Penelitian preklinik, yang juga dipermasalahkan BPOM, sebaiknya dilakukan dengan pendampingan Kemenristek/BRIN.